2.1. Стеклообразное состояние и отличительные свойства стекол
2.2. Основные физико-химические свойства стекол
2.3. Кварцевое стекло, основные методы его получения и свойства
2.1. Стеклообразное состояние и отличительные свойства стекол
Основные требования к материалам, используемым для изготовления ОВ, следующие:
· эти материалы должны быть прозрачными в диапазоне рабочих длин волн;
· они должны вытягиваться в виде тонких нитей;
· должны быть распространенными и относительно дешевыми.
Лучше всего этим требованиям отвечают стекла, и поэтому наибольшее применение получили стеклянные ОВ на основе стекол: кварцевого, фторидного, халькогенидного и т.д. На рис. 2.1 показаны спектральные диапазоны работы ОВ, изготовленных из различных материалов.
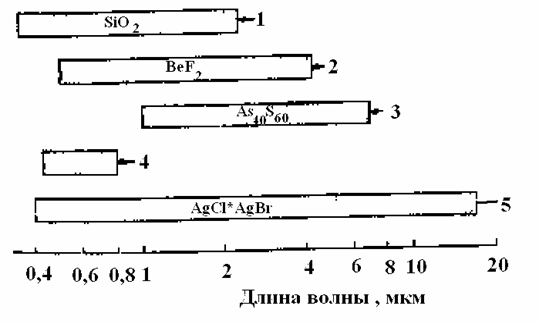
Рис. 2.1. Спектральные рабочие диапазоны ОВ, изготовленных из различных материалов: 1 – кварцевое стекло, 2 – фторидные стекла, 3 – халькогенидные стекла, 4 – полимерные материалы, 5 – галогениды таллия, серебра и т.д.
Общепризнанно существование в природе трех агрегатных состояний веществ: газообразное, жидкое и твердое. Иногда к четвертому состоянию относят плазму. Вещества в твердом состоянии при обычной температуре и давлении могут иметь кристаллическое или аморфное состояние. В природе наиболее распространены кристаллические твердые вещества, для структуры которых характерен геометрически строгий порядок расположения частиц (атомов, ионов) в трехмерном пространстве. Кристаллическое состояние является стабильным при обычных условиях и характеризуется наиболее низкой внутренней энергией. Твердые кристаллические вещества имеют четкие геометрические формы, определенные температуры плавления, в большинстве случаев проявляют анизотропию, т. е. их физические свойства (показатель преломления, теплопроводность, скорости роста и растворения и т. д.) неодинаковы в различных направлениях.
Стеклообразное состояние вещества представляет собой аморфную разновидность твердого состояния и является метастабильным, т. е. характеризуется избытком внутренней энергии. Пространственное расположение частиц вещества, находящегося в стеклообразном состоянии, является неупорядоченным, что подтверждается результатами рентгеноструктурных исследований.
Согласно законам химической термодинамики переход вещества из стеклообразного состояния в кристаллическое должен осуществляться самопроизвольно, однако высокая вязкость твердых веществ делает невозможным поступательные движения частиц, направленное на перестройку структуры. В твердых телах совершаются только колебательные движения относительно равновесия.
Согласно определению комиссии по терминологии АН СССР (1932 г.) стеклом называются все аморфные тела, получаемые путем переохлаждения расплава независимо от их состава и температурной области затвердевания и обладающие в результате постепенного увеличения вязкости механическими свойствами твердых тел, причем процесс перехода из жидкого состояния в стеклообразное должен быть обратимым.
Все типы стекол независимо от их химического состава и температурной области затвердевания обладают специфическими свойствами, которые отличают их от кристаллов и жидкостей.
1. Стекла рентгеноаморфны вследствие неупорядоченного атомного строения. В структуре стекла отсутствует дальний порядок, т. е. систематическая повторяемость элементарных объемов структуры, характерная для кристаллических веществ.
Основной структурной единицей кварцевого стекла является кремнекислородный тетраэдр (рис. 2.2), где атом кремния окружен четырьмя атомами кислорода., расположенных симметрично в вершинах тетраэдра.
Образование группировки обусловлено координационными требованиями атомов кремния, учитывающими соотношение геометрических размеров атомов. При соотношении ионных радиусов катиона и аниона (rk/ra) в интервале 0,225 – 0,414 координационная группировка имеет тетраэдрическое расположение атомов. В SiO2 – rk/ra =0,29. Геометрические размеры связей приведены на рис. 2.2.
Структура кварцевого стекла выполнена из тетраэдров [SiO4]-4, соединенных друг с другом вершинами через атомы кислорода. В результате образуется непрерывный пространственный каркас, отличающийся от геометрически правильных решеток кристаллических модификаций кварца отсутствием дальнего порядка. Тетраэдры [SiO4]-4 не образуют в пространстве правильных сочленений (рис. 2.2, в) в виде шестигранных колец, характерных для структуры высокотемпературного кристаболита, а структурная решетка стекла выглядит как искаженная кристаллическая решетка. Искажение заключается в произвольном варьировании угла связи Si-O-Si между соседними тетраэдрами в структуре цикла с наиболее вероятным значением ![]() 0.
0.
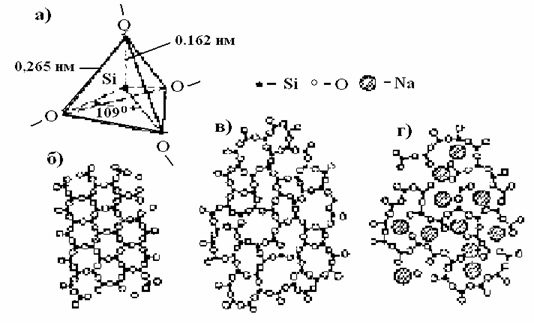
Рис. 2.2. Тетраэдрическая группировка (SiO4)-4 (а) и схематическое изображение на плоскости сочленения тетраэдров в структуре кристаллического (б) и стеклообразного кварца (в), а также силикатного стекла (г)
Группировка [SiO4]-4 имеет избыточный отрицательный заряд (-4), но каркасная сетка из тетраэдров в целом электронейтральна, т. к. каждый атом О связан с двумя атомами Si. В структуре кварцевого стекла все атомы О – мостиковые. Структуры кристаллической и стеклообразной форм SiO2 не являются плотноупакованными, т. к. тетраэдры соединяются вершинами, а не ребрами и гранями. Поэтому в кварцевом стекле имеются свободные полости, что обуславливает высокую газопроницаемость кварцевого стекла по сравнению с другими силикатными стеклами, в которых присутствуют оксиды щелочных и щелочно-земельных металлов, располагающихся в области полостей (рис. 2.2 г). Компоненты стекол, которые способны самостоятельно образовывать непрерывную структуру стекла, называются стеклообразователями. К ним относятся SiO2, GtO2, P2O5, B2O3 и т.д. Компоненты стекла, не способные самостоятельно образовывать непрерывную структурную сетку, называются модификаторами. Это обычно оксиды элементов I и II групп периодической системы элементов Д.И.Менделеева.
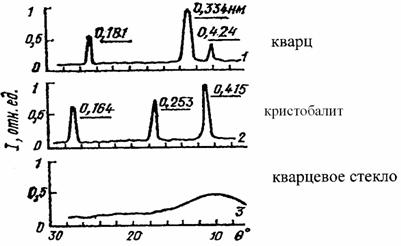
Рис. 2.3. Рентенограммы кристаллического кварца (а), кристобалита (б) и кварцевого стекла
На рис. 2.3 показаны рентгенограммы кристаллического кварца (1), кристобалита – высокотемпературной модификации кварца (2) и кварцевого стекла(3). Из рисунка видно, что в отличие от кристаллических модификаций для стеклообразного вещества наблюдается широкая диффузная полоса характерная для аморфных структур (называемая «аморфное гало»). Периодическое расположение частиц в структуре кристаллов на расстояниях d, сопоставимых с длиной волны рентгеновского излучения λ, обуславливает появление на ренгенограммах дифракционных максимумов под углами скольжения θ,определяемыми из уравнения Вульфа-Брегга:
![]() (2.1),
(2.1),
где n - порядок отражения. Отсутствие на рентгенограммах стекол интенсивного рассеяния под малыми углами, характерного для газов или аморфных гелей с размерами частиц 1-10 нм, свидетельствуют об однородном и непрерывном строении стекол. Если ориентировочно определить межплоскостное расстояние, соответствующее максимуму аморфного гало, то оно оказывается близким к дифракционному максимуму кристобалита – 0.415 нм, что соответствует связи Si-O.
2. Стекла изотропны, если они однородны по составу, свободны от напряжений и дефектов. Изотропия свойств стекол, как и других аморфных средств, обусловлена отсутствием направленной в пространстве ориентации частиц.
3. Стекла не имеют определенной температуры затвердевания или плавления. Оба эти процесса происходят постепенно в некотором температурном интервале. При охлаждении расплав переходит из жидкого в пластическое состояние, и только затем в твердое (процесс стеклования). Наоборот, при нагревании стекло переходит из твердого в пластическое состояние, а при более высокой температуре - в жидкое (размягчение стекла). Температурный интервал, в котором происходит процесс стеклования или обратный ему процесс размягчения, называется интервалом стеклования и ограничен двумя температурами: со стороны высоких температур – Tf в немецкоязычной литературе (от слова flussig – жидкий) или Ts в англоязычной литературе (от слова "soft" -мягкий), cо стороны низких температур –Tg (от слова "glass" – стекло). При Tg стекло обладает свойствами твердого упругого тела с хрупким разрушением, а температура Tf (Ts) – это граница пластического или жидкого состояния и при Tf удается вытягивать из стекломассы тонкие нити.
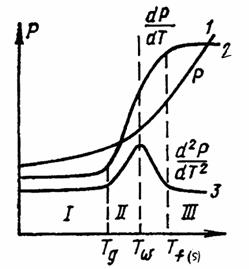
Рис. 2.4. Зависимости свойств стекол от температуры: 1 – P (T,V,H,S,η,ρ), 2 – dP/dT (KTP,C), 3 – d2P/dT2 (ά,ε)
Процессы размягчения стекла или затвердения стекломассы являются однофазными, в отличие от плавления кристаллических веществ или кристаллизации расплавов. При размягчении стекла в интервале стеклования отсутствует жидкая фаза.
Свойства стекол по характеру изменения в интервале стеклования делятся на три группы (рис.2.4):
· свойства (P), характеризующие функцию состояния вещества (внутренняя энергия Е, мольный объем V, энтальпия Н, энтропия S) и кинетические свойства (вязкость ![]() , удельное сопротивление
, удельное сопротивление ![]() ), которые меняются постепенно с ростом Т;
), которые меняются постепенно с ростом Т;
· свойства, представляющие первую производную по температуре (dP/dT) от свойств первой группы (КЛТР, теплоемкость), имеют точку перегиба при Тw;
· свойства (теплопроводность, диэлектрические потери), которые являются вторыми производными d2P/dT2 и имеют экстремальные значения при Tw.
Характер изменения свойств стекол при нагревании существенно отличается от температурных зависимостей сплавов кристаллических веществ, которые имеют резкое скачкообразное изменение при Тпл, как это видно на рис. 2.5.
Температуры Тg и Tf принадлежат к числу характеристических точек на температурной кривой вязкости. Tg соответствует вязкости стекломассы, равной 1012,.3 Па×с (или 1013,3 пз); а Tf – вязкости 108 Па×с (или 107,6 пз). Для кварцевого стекла ![]() и
и ![]() . При вязкости более 1012,3 (< Tg ) стекло представляет собой твердое хрупкое тело, а при T>Tf стекломасса находиться в расплавленном состоянии.
. При вязкости более 1012,3 (< Tg ) стекло представляет собой твердое хрупкое тело, а при T>Tf стекломасса находиться в расплавленном состоянии.
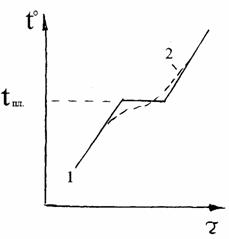
Рис. 2.5. Зависимость температуры образца от времени повышения температуры нагрева: 1 – для кристаллов, 2 – для стекол
4. Свойства стекол зависят от скорости переохлаждения (или нагревания). При малой скорости охлаждения при достижении Ткр. происходит кристаллизация расплава. При высокой скорости переохлаждения расплав может миновать Ткр. без кристаллизации и находиться в «метастабильном» состоянии «переохлажденной жидкости». При нагревании стекло стремится перейти в термодинамически устойчивое состояние, что может быть достигнуто в результате фазового разделения. Фазовое разделение можетосуществляться путем кристаллизации или ликвации стекол. Вследствие высокой вязкости стекломассы процессы фазового разделения не достигают полного завершения, и обычно существуют 2 фазы:
при кристаллизации - кристаллической и стекловидной;
при ликвации – 2 стекловидные с различными соединениями компонентов.
5. Стекла расплавляются и отвердевают обратимо.
Механизм кристаллизации при переохлаждении расплава включает 2 стадии: образование центров (ОЦ) кристаллизации (зародышей) и рост кристаллов (РК) на них. Центры кристаллизации – это микрочастицы с упорядоченным порядком и структурой, которую могут зарождаться гомогенно в результате локальных флуктуаций состава и структуры. Гетерогенная кристаллизация происходит на примесных центрах инородной фазы. Скорости ОЦ и РК зависят от температуры (или переохлаждения), и максимумы этих зависимостей могут не совпадать, как это видно из рис. 2.6.
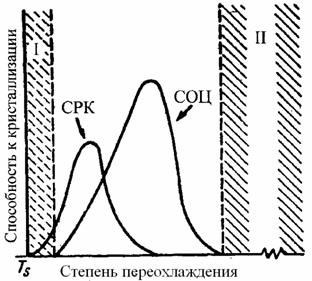
Рис. 2.6. Скорость образования центров кристаллизации (СОЦ) и скорости роста кристаллов (СРК) как функция степени переохлаждения вязкого расплава
Стеклообразное состояние более устойчивое для систем, у которых эти максимумы раздвинуты широко и малы по величине. Выявлено для двойных, тройных и более сложных расплавов, что чем больше количество стеклообразователя (высоковязкого компонента), тем сильнее выражена склонность системы к стеклообразованию. Стеклообразователи (SiO2, P2O5, B2O3, GeO2) – это компоненты, способные самостоятельно образовывать непрерывную структурную сетку. Вязкость некоторых веществ, в том числе стеклообразователей, приведена в таблице 2.1, из которой видно, что все стеклообразователи, находящиеся в правой части таблицы, имеют высокую вязкость, в то время как, например, переохлажденная вода остается маловязкой жидкостью.
Таблица 2.1 Вязкость некоторых веществ при температурах плавления
|
Вещество |
Температура плавления,0С |
Вязкость, пз |
Вещество |
Температура плавления, 0С |
Вязкость, пз |
|
Na Fe H2O Al2O3 LiCl |
98 1535 0 2050 613 |
0,01 0,07 0,02 0,6 0,02 |
SiO2 GeO2 B2O3 As2O3 BeF2 |
1710 1115 450 309 540 |
107,7 105,4 105 106 106 |
2.2. Основные физико-химические свойства стекол
2.2.1. Вязкость
Вязкость – это свойство жидкостей оказывать сопротивление перемещению одной части жидкости относительно другой. Согласно постулату Ньютона сила F, необходимая для поддержания постоянной разницы скоростей между двумя движущимися параллельно слоями жидкости, равна
![]() (2.1),
(2.1),
где η – динамическая вязкость, S – поверхность раздела, ![]() - градиент скорости, т.е. изменение скорости на единицу расстояния. Кроме динамической вязкости существует понятие кинематической вязкости, которая записывается как
- градиент скорости, т.е. изменение скорости на единицу расстояния. Кроме динамической вязкости существует понятие кинематической вязкости, которая записывается как
![]() (2.2),
(2.2),
где ![]() -плотность.
-плотность.
Скорость течения жидкостей, подчиняющихся закону Ньютона (ньютоновские или нормальные жидкости), пропорциональна давлению, и при ламинарном потоке pt=const, т.е. вязкость ньютоновских жидкостей не зависит от давления, оказываемого на жидкость. Для коллоидных растворов и суспензий ή уменьшается с ростом давления, что обусловлено связями между дисперсными частицами.
Изменения вязкости жидкости нормальных жидкостей от температуры выражается уравнением Френкеля – Андраде:
![]()
![]() (2.3),
(2.3),
где ![]() - энергия активации процесса течения, R – универсальная газовая постоянная, равная 8,31´103 дж/(кмоль×град)=1,987 ккал/(моль×град). Величина энергии активации отражает силу взаимодействия между атомами и определяется работой, которую надо затратить атому, чтобы перейти из одного положения в другое. В отличие от кристаллических тел в стеклах энергия активации не является постоянной величиной, а изменяется с изменением температуры стекла, как это видно из таблицы 2.2.
- энергия активации процесса течения, R – универсальная газовая постоянная, равная 8,31´103 дж/(кмоль×град)=1,987 ккал/(моль×град). Величина энергии активации отражает силу взаимодействия между атомами и определяется работой, которую надо затратить атому, чтобы перейти из одного положения в другое. В отличие от кристаллических тел в стеклах энергия активации не является постоянной величиной, а изменяется с изменением температуры стекла, как это видно из таблицы 2.2.
Таблица 2.2 Изменение энергии активации кварцевого и боратного стекол.
|
B2O3 |
SiO2 |
||
|
Температура, 0С |
Энергия активации, ккал/моль |
Температура, 0С |
Энергия активации, ккал/моль |
|
260 |
83 |
1300-1450 |
170±8 |
|
315 |
64 |
1720-2000 |
151±10 |
|
450 |
40 |
1925-2060 |
134±9 |
|
500 |
38 |
1935-2320 |
89±21 |
|
600 |
30 |
||
Согласно теории Мюллера факт изменения энергии активации от температуры для стекол объясняется тем, что при течении вязких расплавов происходит не разрыв ковалентной связи (например, Si-O, B-O), а их переключение (трансляция), т.е. они имеют как бы шарнирный характер.
В узком интервале температур зависимость вязкости от температуры обычно записывают как:
![]() (2.4),
(2.4),
где А и В – некие постоянные величины для каждого стекла. Отжиг заготовок происходит вблизи Тg, (где lgh=13,3 пз), а вытяжка волокна в области Tf (где lgh=7,6 пз). Вязкость стекла значительно зависит от его состава. Для примера, на рис. приведены зависимости температуры размягчения кварцевого стекла при его легировании рядом примесей, которые наиболее широко используются при изготовлении кварцевых ОВ.
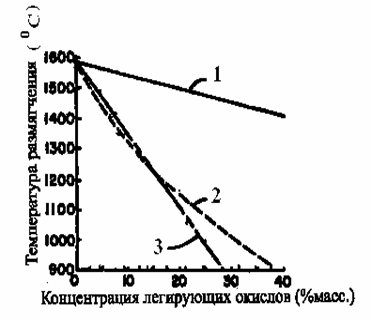
Рис. 2.7. Зависимости температуры размягчения легированного кварцевого стекла в зависимости от его состава и концентрации легирующих компонентов: 1 – SiO2*GeO2, 2 – SiO2*P2O5, 3 – SiO2*B2o3
Из рис. 2.7 видно, что при увеличении концентрации примесей во всех случаях наблюдается уменьшение температуры размягчения (т.е. вязкости стекла), причем легирование P2O5 или B2O3 влияет на вязкость стекла сильнее, чем GeO2.
Это объясняется тем, что при легировании GeO2 он встраивается в решетку SiO2, а при легировании Р2О5 и B2О3, связи нарушаются, ослабевают и вязкость падает.
2.2.2. Поверхностное натяжение
Поверхностное натяжение расплавов и твердых тел определяет действие межмолекулярных сил на частицы поверхности слоя среды. Мерой поверхностного натяжения в (Дж/м2 или Н/м) является работа А, которую необходимо затратить на образование единицы поверхности среды S, т.е.
s= А/S (2.6).
Действие поверхностного натяжения направлено на уменьшение площади поверхности. Для промышленных стекол s = 0,159 ![]() 0,470 Н/м, а для кварцевого стекла составляет ~ 0,4 Н/м. Поверхностное натяжение мало зависит от температуры.
0,470 Н/м, а для кварцевого стекла составляет ~ 0,4 Н/м. Поверхностное натяжение мало зависит от температуры.
2.2.3. Показатель преломления
Способность стекла преломлять падающий на него свет принято характеризовать посредством показателя преломления (ПП) для прямого луча, испускаемого либо парами натрия (λ=5893А), либо светящимся в гейслеровой трубке гелием (l=5875 А). Как было показано выше (уравнение 1.12), ПП характеризует также скорость распространения света в материале по отношению к скорости света в вакууме. Для чистого кварцевого стекла принято считать ПП в ближней ИК-области при комнатной температуре равным n=1,458.
2.2.4. Термическое расширение
Термическое расширение оценивается коэффициентами линейного термического расширения (КЛТР), которые рассчитываются по формуле:
![]() или
или ![]() (1/град)
(1/град)
КЛТР сильно зависят от состава стекла. Поэтому при выборе конструкции ОВ необходимо учитывать КЛТР оболочки и сердцевины с тем, чтобы не допустить сильных напряжений на границе между ними, ибо эти напряжения могут привести к разрушению ОВ.
2.3. Кварцевое стекло, основные методы его получения и свойства
ОВ на основе кварцевого стекла получили в настоящее время наибольшее распространение. Это связано с тем, что:
- кварцевое стекло является моносоединением и обладает большой химической устойчивостью и высокой механической прочность,
- соединения, из которых может быть получено кварцевое стекло широко распространены (это песок, горный хрусталь и т.д.),
- разработана технология получения высокочистых соединений кремния (прежде всего тетрахлорида кремния и тетраэтоксисилана), на основе которых может быть получено кварцевое стекло очень высокой степени чистоты.
Структуру кварцевого стекла подробно рассматривали в разделе 2.1.1, поэтому здесь остановимся на исходных материалах и методах получения кварцевого стекла, которые определяют содержание в нем примесей. Исходными материалами для получения кварцевого стекла являются: природные виды кварца (горный хрусталь и его разновидности, жильный кварц и т.д.); искусственные кристаллы кварца, выращенные гидротермальным способом в автоклавах; тетрахлорид кремния. При использовании природного кварца и искусственных кристаллов они дробятся, промываются в смеси кислот HCl+HNO3 и в воде, где с поверхности удаляются неорганические загрязнения, а сама двуокись кремния не растворима в этих кислотах. Полученную крупку перебирают, удаляя частицы, содержащие различные включения, после чего наплавляют в блоки. Используют следующие методы наплава:
1. электротермический наплав крупки в атмосфере Н2,
2. газопламенный наплав в пламени О2-Н2 горелки,
3. электротермический наплав крупки в вакууме,
4. парофазный гидролиз SiCl4 в пламени О2-Н2 горелки,
5. окисление SiCl4 в кислородной ВЧ-плазме.
В таблице 2.3 приведено содержание примесей переходных металлов и гидроксильных групп в кварцевом стекле опорных труб, полученном вышеуказанными методами.
Таблица 2.3 Содержание примесей переходных металлов и гидроксильных групп в трубах из кварцевого стекла, полученного вышеуказанными методами
|
Метод получения |
Содержание примесей масс. % |
||||||
|
Fe |
Cr |
Ni |
Mn |
Cu |
Co |
OH |
|
|
1. 2. 3. 4. 5. 6. |
2×10-4 4×10-5 8×10-5 1×10-5 2×10-5 3×10-5 |
4×10-6 3×10-6 5×10-6 <3×10-6 3×10-6 3×10-6 |
5×10-5 4×10-6 5×10-6 3×10-6 <1×10-6 <1×10-7 |
6×10-6 2×10-6 1×10-6 1×10-6 1×10-6 9×10-7 |
5×10-5 4×10-6 3×10-6 5×10-6 3×10-7 <1×10-7 |
3×10-6 <2×10-7 <2×10-7 <2×10-6 <2×10-7 <2×10-7 |
2×10-2 3,5×10-2 2×10-4 1,2×10-1 2×10-4 1,5×10-8 |
Примечание: в строке 6 приведены данные для труб "Suprasil F-300" фирмы "Heraeus", полученных из заготовок, произведенных методом OVD.
Видно, что содержание примесей переходных металлов значительно выше в первых трех типах труб по сравнению со стеклом, полученным из SiCl4, а концентрация ОН-групп ниже в стеклах, полученных наплавом в вакууме или в ВЧ-плазме.
![]()

Рис. 2.8. Спектральные зависимости оптических потерь в ОВ с германосиликатной сердцевиной и светоотражающей оболочкой из кварцевого стекла, полученного различными технологиями: 1- электротермический наплав в Н2, 2 – газопламенный наплав, 3 – электротермический наплав в вакууме, 4- парофазный гидролиз.
На рис. 2.8 приведены типичные спектральные зависимости потерь в ОВ, при изготовлении которых (в ИХВВ РАН) германосиликатная сердцевина формировалась методом MCVD, а отражающей оболочкой служил материал кварцевых труб, соответствующих нумерации таблицы 7. Видно, что в образцах 1 и 3, характеризующихся большой концентрацией Fe, Cr, Mn, потери больше в ближнем ИК- диапазоне, а большие потери на l=1,38 мкм характерны для стекол, при изготовлении которых применялся Н2 (образцы 1, 2, 4). Особняком стоит стекло "Suprasil F-300", имеющее наименьшую концентрацию примесей переходных металлов и гидроксильных групп. Поэтому эти трубы широко используются во всем мире для получения ОВ с минимальными потерями.
По светопропусканию кварцевые стекла делят на КУ, КВ, КИ, КУВИ, отличающиеся составом и концентрацией примесей. Стекла КУ предназначены для работы в УФ-диапазоне спектра и содержат большое количества ОН-групп (до ~ 0,1 масс. %). Стекла КВ предназначены для работы в видимой области спектра, КИ – для инфракрасной области, и поэтому последние содержат малое количество гидроксильных ионов. Для примера на рис. 2.9 приведены спектральные зависимости коэффициента пропускания для стекол КУ и КИ.
Существуют 2 основных способа производства кварцевых труб:
- одностадийный, когда крупка или блок стекла поступает в молибденовую печь, снизу которой установлены пуассон и дуза, которые определяют наружный и внутренний диаметры трубки;
двухстадийный, при котором сначала наплавляют блок стекла, затем его обрабатывают механически, протыкая блок и затем шлифуя его внутреннюю и наружную поверхности таким образом, чтобы получить необходимое соотношение внутреннего и наружного диаметров в трубке. После механической обработки блок перетягивают в трубы в графитовой печи методом подобия.
Первый метод более прост, обеспечивает непрерывный процесс вытяжки труб и их относительно хорошую геометрию. Недостатком метода является загрязнение его молибденом, в результате чего прочность ОВ резко снижает ся. Сейчас трубки, полученные этим способом, для производства заготовок ОВ не используются. Преимущество второго способа состоит в том, что блок стекла не контактирует с элементами печи и не подвергается загрязнению. Кроме того этот способ позволяет получать трубы очень хорошей геометрии, Например, трубы фирмы "Heraeus" 20´2 мм имеют среднестатистическое отклонение наружного диаметра не более 0,08 мм, толщины стенки – не более 0,02 мм, разнотолщинность и овальность - не более 0,01 мм и т.д.
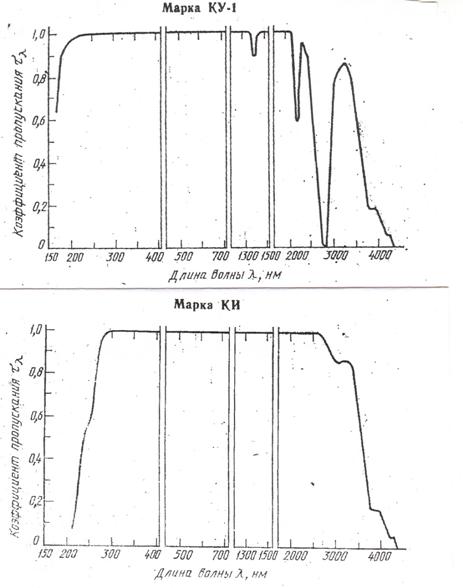
Рис. 2.9. Спектральные зависимости коэффициента пропускания кварцевых стекол марки КУ-1 и КИ.
Таблица 2.4 Основные свойства кварцевого стекла
|
Свойство |
Значение |
|
Плотность, (г/см3) Показатель преломления Коэффициент линейного термического расширения, (град-1) Теплоемкость, (кал/г*град) Теплопроводность, (кал/см*град) Микротвердость, (кг/мм2) Прочность, (кг/мм2): стержней волокон |
2,20 1,458 5,7´10-7 0,177 0,0033 703 7 1200 |
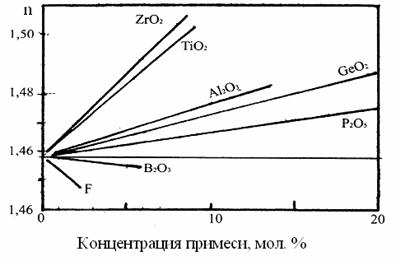
Рис. 2.10. Зависимости показателя преломления кварцевого стекла от концентрации легирующих примесей.
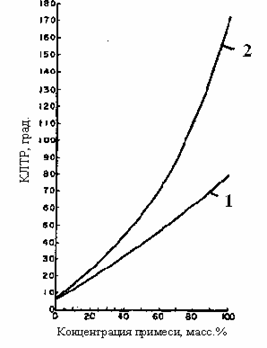
Рис. 2.11. Зависимости КЛТР кварцевого стекла от концентрации легирующих примесей:
1 – GeO2 , 2 – B2O3
Свойства кварцевого стекла можно менять путем его легирования. Так, на рис. 2.10 приведены зависимости ПП кварцевого стекла от концентрации различных легирующих компонентов, применяемых при получении заготовок ОВ. Видно, что имеются только два компонента, которые уменьшают ПП кварцевого стекла (В2О3 и F), и потому их часто используются для формирования светоотражающей оболочки. Остальные примеси увеличивают ПП кварцевого стекла и потому их обычно используются для формирования световедущей сердцевины (особенно GeO2 и P2O5).
Легирование кварцевого стекла изменяет также и вязкость стекла (см. рис. 2.7) и КЛТР, как это видно из рис. 2.11. Введение В2О3 вызывает значительно большее изменение КЛТР, чем GeO2, что используется при получении заготовок ОВ, сохраняющих поляризацию излучения. Таким образом, варьируя состав кварцевого стекла и концентрацию легирующих компонентов можно изменять свойства кварцевого стекла и получать ОВ различного типа и назначения.

